β-(1→3)結合を主鎖に持つ多糖は、キノコや菌類や藻類および植物の構造多糖あるいは貯蔵多糖として、広く自然界に存在する天然高分子です。生理活性などの機能解析が活発に行われた結果、免疫賦活作用に基づく抗腫瘍活性など興味深い薬理活性を示すことが判明し、レンチナン(シイタケ)、シゾフィラン(スエヒロタケ)、クレスチン(カワラタケ)といった医薬品が誕生しました。また、最近では核酸とシゾフィランがそれぞれ1本と2本からなる3重らせんを形成しうることが見出され、遺伝子マニピュレーターとしての機能も期待されていることから、(1→3)-β-D-グルカンは機能性高分子材料として大変興味深い物質群と言えます。
近年でも様々なキノコ類から相次いで高活性な多糖成分が抽出されています。”β-グルカン”といいう名で広く一般に知られるこれらの多糖成分は様々な分岐間隔で単糖、オリゴ糖及びペプチド側鎖を有することが示唆されており、(1→3)-β-D-グルカンの分岐機構と薬理活性との相関に関心が集まっています。しかし、その多くは側鎖が単一でないため、シゾフィランなど単糖を側鎖に有するものと違い、その機能がどの構造に由来するかをとくていすることが困難な状況となっています。この”β-グルカン”の構造と機能との相関を明確にするには、単一な側鎖構造を有するモデル多糖を用いてそれぞれの生理活性を評価してやればよいのですが、そのような多糖の合成は非常に困難で、ほとんど成功例がないというのが実情です。
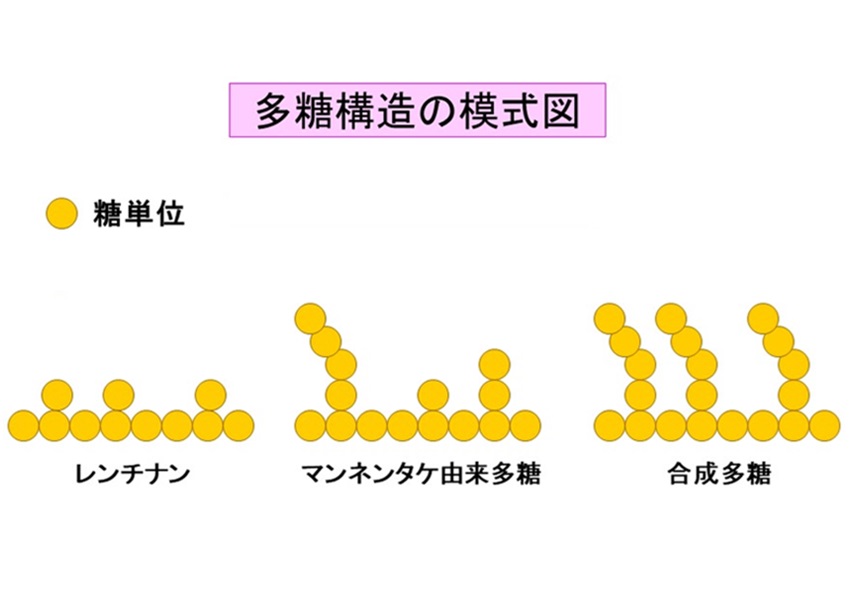
ただし、多くの多糖は、下の模式図に示してあるように側鎖が単一でないため、レンチナンなど単糖を側鎖に有するものと違い、その機能がどの構造に由来するかを特定することが困難な状況となっています。例として、構造が明らかにされているマンネンタケ由来多糖についてご覧下さい1。従って、化学合成を用いて構造が明確なモデル多糖を合成し、その機能を解析することが必要となる訳なのですが、そのような分岐型(1→3)-β-D-グルカンの合成は極めて困難であり、側鎖のない(1→3)-β-D-グルカンの化学合成ですら、速報で1例しか報告されていない状態です2。ゆえに、本研究では1,3-アンヒドロ糖誘導体の開環重合を基盤としてβ(1→3) 結合を主鎖にもつ生理活性多糖を様々に合成し、構造と機能の詳細な相関解析を目的としました。
論文発表はまだですが目的とする分岐型(1→3)-β-D-グルカンがいくつか合成され、免疫活性の検討も始まっています。今後の進展にご期待下さい。
- X. Bao, C. Liu, J. Fang, and X. Li, Carbohydr. Res., 332, 67-74 (2001).
- M. Okada, Y. Yamakawa, and H. Sumitomo, Macromolecules, 24, 6797-6799 (1991).
